Первая университетская клиника: мы лечим не органы, а пациента №6(100), 2019 год
Опытные врачи Первой университетской клиники круглосуточно готовы оказать высококвалифицированную помощь как в проведении диагностики, так и в лечении терапевтических, хирургических, гинекологических, урологических, неврологических, онкологических, онкогематологических заболеваний. Эта многопрофильная медицинская клиника расположена в центре Москвы. «Профессионализм, индивидуальный подход, внимание и забота о каждом пациенте — наши принципы, которыми мы руководствуемся каждый день», — утверждает руководитель клиники Анна Сидорова.
— В основе нашей деятельности лежат лучшие традиции академического подхода к лечению: все используемые нами методы научно обоснованы и признаны. При этом мы продолжаем внимательно следить за развитием медицины, в борьбе с заболеваниями применяем новейшие разработки, которые используются в самых современных клиниках Европы и США, — рассказывает Анна Юрьевна. — Коллектив врачей клиники состоит из специалистов, получивших фундаментальное медицинское образование в лучших вузах страны. При этом все наши специалисты постоянно повышают свою квалификацию, особое внимание уделяется сертификации, аттестации медицинского персонала, согласно государственным стандартам оказания медицинской помощи. В составе клиники — отделения эндоскопии, неврологии и восстановительного лечения, терапии, кардиологии, эндокринологии, урологии, онкологии, химиотерапии, лучевой терапии, паллиативной помощи, хирургическое отделение. Работает круглосуточный стационар, оснащённый новейшим оборудованием. Нашим пациентам доступна ультразвуковая и функциональная диагностика, рентгенография, рентгеноскопия, магниторезонансная томография, компьютерная томография; выполнение биопсии любой сложности, верификация диагноза с проведением цитологического, гистологического, иммуногистохимического и молекулярного исследования. Диагностика проводится с использованием инновационных инструментальных и лабораторных методов. Для точности исследований, постановки диагноза и лечения принципиально важна современная и высокоточная аппаратура. В нашей клинике используется аппаратура экспертного класса, что гарантирует пациенту медицинскую помощь самого высокого качества.
Специалисты клиники проводят лечение острых и хронических тромбозов, в том числе флотирующих, лечение почечной и печёночной недостаточности, плевритов и асцитов, проводят подбор самых эффективных схем лечения с учётом индивидуальных особенностей пациента, возраста и сопутствующей патологии с привлечением ведущих экспертов страны и зарубежных коллег.
Для успешного лечения важно понимание того, что каждый пациент индивидуален, все органы в его организме работают в тесной взаимосвязи друг с другом и зависят от личных особенностей больного, поэтому мы лечим не органы, а пациента: проводим подбор индивидуальной программы реабилитации после инсульта, инфаркта, обезболивания, восстановления после хирургического, лучевого, химиотерапевтического лечения. В лечении нами используются только самые современные и передовые методы: химиотерапия, гормонотерапия, таргетная терапия, иммунотерапия, сочетанная химиолучевая терапия; мы применяем исключительно оригинальные и эффективные колониестимулирующие агенты.
Пациент может позвонить врачу в любое время суток и получить помощь или консультацию.
Нам важно не просто выполнить ряд манипуляций, но действительно вылечить человека, с тем чтобы он вернулся к здоровой и полноценной жизни.
Диагностика РМЖ обеспечивает раннее выявление заболевания, что является залогом успешного лечения, считает Гаяне Геворковна Казарян, врач ультразвуковой диагностики высшей категории со стажем работы более 10 лет, соискатель учёной степени кандидата медицинских наук.
— Рак молочной железы представляет собой злокачественную опухоль железистой ткани молочной железы и является наиболее частой формой рака среди женщин, каждая десятая женщина подвержена риску заболевания, в зависимости от возраста и региона проживания. В популяции рак молочной железы занимает второе место среди онкологических заболеваний после рака лёгкого. Ежедневно в мире регистрируются более 3830 новых случаев рака молочной железы, это 2,7 случая в минуту. Риск возникновения патологии увеличивается с возрастом, большая часть пациентов (77 %) старше 50 лет, на долю молодых девушек приходится 0,3 %.
Неоценим вклад зарубежных и отечественных онкологов в совершенствование методов диагностики и лечения рака молочной железы. Ежедневно ведутся разработки новых методик лечения.
В последние три десятилетия наряду с совершенствованием лечения проводятся программы по изучению эффективности различных методов, направленных на более раннее выявление злокачественных опухолей молочных желёз.
По мнению экспертов ВОЗ, наиболее перспективный подход для сокращения смертности от РМЖ — проведение мероприятий по раннему выявлению заболевания. Учёными установлена высокая эффективность маммографического и ультразвукового скрининга РМЖ. Более дешёвые программы скрининга, такие как самообследование, не показали своей эффективности.
Скрининговые программы хорошо развиты в Швеции, Норвегии, Голландии, Бельгии. И сегодня опыт этих стран даёт нам возможность говорить о реальности снижения смертности от РМЖ на 30 %.
В мире «золотым стандартом» скрининга РМЖ является маммография, проведение которой позволяет снизить смертность на 30–50 %. Качественный маммографический скрининг РМЖ, по данным ВОЗ, предполагает наличие парка современного диагностического оборудования (комплексы для выполнения стереотаксической биопсии непальпируемых опухолей, высокочувствительные ультразвуковые аппараты), активное участие в скрининге женского населения (>75 % популяции), направление на скрининг только здоровых, не предъявляющих жалоб женщин, возраст обследуемых 40–69 или 50–69 лет; наличие Канцер-регистра — для учёта показателей заболеваемости и смертности.
Система скрининга — сложная многоуровневая структура. При этом маммографическое исследование только первый отборочный этап профилактического обследования практически здорового населения для выявления лиц, имеющих скрыто протекающие заболевания. Следующий этап — это ультразвуковое исследование, которое также широко используется при реализации скрининговой программы по ранней диагностике РМЖ. Среди женского населения в возрасте до 40 лет данный метод обследования является единственно возможным скрининговым тестом. Наибольшую ценность, однако, представляет выявление очаговой доброкачественной патологии у женщин указанной возрастной категории. Последующее обязательное лечение предопухолевых заболеваний является мерой первичной профилактики, направленной на снижение заболеваемости РМЖ.
В последние годы наряду с использованием серошкального режима широкое применение получило ультразвуковое исследование с использованием цветового доплеровского и энергетического картирования, эластографии и ультразвукового контрастирования. Ультразвуковое исследование является высокоэффективным методом распознавания рака молочной железы.
Метод не имеет противопоказаний, не даёт лучевой нагрузки и позволяет проводить прицельную пункционную биопсию опухолей молочной железы.
Ультразвуковое исследование выполняется в масштабе реального времени с помощью датчиков 9–12 МГц. Обязательно исследуются обе молочные железы в горизонтальном положении, в положении на боку, сидя, с поднятой рукой на исследуемой стороне. Наиболее частыми эхографическими признаками опухоли являются сниженная эхогенность и неоднородность внутренней структуры узла, неровные и нечёткие контуры, дорсальная акустическая тень, наличие микро- и макрокальцинатов. При цветовом доплеровском и энергетическом картировании выявляется разной степени васкуляризация опухоли. Чувствительность УЗИ в выявлении рака молочной железы составляет почти 89,8 %. Использование в сложных для диагностики случаях доплерографии, эластографии, контрастирования и пункционной биопсии опухолей под контролем УЗИ позволяет установить правильный диагноз и повысить чувствительность ультразвукового исследования с 89,8 % до 97 %.
Стоит отметить, что только комплексная диагностика, включающая маммографию, ультразвуковое исследование, ультразвуковую ангиографию, позволяет получить максимально уточнённый диагноз, разработать более точные рекомендации для оперативного лечения больных. Разработанные дифференциально-диагностические критерии злокачественных и доброкачественных образований, а также определение распространённости опухолевого процесса молочной железы позволяют в каждом конкретном случае подобрать адекватное лечение в короткий срок. При комплексном применении всех вышеуказанных методов лучевого исследования чувствительность составляет 93,8 %, специфичность — 88,6 %.
Шкала BI-RADS позволяет расставить правильные акценты при формировании ультразвукового заключения, указывая конкретный план дальнейших медицинских действий, направленных на постановку окончательного диагноза, выработку тактики ведения пациенток с образованиями молочных желёз.
Breast Imaging-Reporting and Data System (BI-RADS) — система описания и обработки данных лучевых исследований молочной железы — разработана Американским колледжем радиологов в сотрудничестве с другими организациями. Шкала BI-RADS предназначена для стандартизации оценки результатов рентгеновской маммографии по степени риска наличия злокачественных образований молочной железы и впоследствии распространена на оценку результатов МР- и УЗ-исследований.
Основой формирования заключения являются данные УЗИ, выполненного в В-режиме. Результаты, полученные с помощью дополнительных методик (ЦДК, ЭК, спектральный анализ кровотока, эластография любого вида и др.), а также выявление изменённых лимфатических узлов в зонах регионарного лимфооттока позволяют более чётко определить категорию (чаще в спорных случаях между категориями 3 и 4 или между подкатегориями последней), чаще в сторону повышения.
Введение системы интерпретации и протоколирования результатов УЗИ молочной железы по шкале BI-RADS в повседневную практику врача ультразвуковой диагностики позволило систематизировать полученные результаты, определить тактику оптимального дальнейшего обследования и ведения пациенток с новообразованиями молочных желёз, обеспечить преемственность лечебно-диагностических мероприятий.
На сегодняшний день лечение планируется на консилиуме с участием хирурга, химиотерапевта и радиолога, после проведения тщательного и полного обследования пациентки, установления стадии заболевания и верификации диагноза путём проведения гистологического и иммуногистохимического исследования. Немаловажно определение сопутствующей патологии, так как предстоящее противоопухолевое лечение зачастую приводит к обострению хронической патологии, а декомпенсация хронических заболеваний является противопоказанием для проведения специфического противоопухолевого лечения.
Целесообразно проведение генетического исследования, если возраст начала заболевания до 40–45 лет, больным с первично множественными опухолями (рак молочной железы и рак яичников; синхронные и метахронные опухоли), пациентки с отягощённым семейным онкологическим анамнезом (рак молочной железы, рак яичников, рак желудка), у пациенток с негативным статусом рецепторов (ER, PR, HER2) — только для BRCA1-ассоциированных опухолей.
На основании данных о стадии опухолевого процесса, биологических особенностях характеристик опухоли оценивается прогноз заболевания и вырабатывается оптимальный план лечения конкретной пациентки. К прогностическим факторам относят размер опухоли, состояние регионарных лимфоузлов, отёк молочной железы, наличие инвазивных свойств протоковой карциномы, степень дифференцировки опухоли, рецепторы эстрогенов, Her2-neu-статус, наличие мутаций BRCA1, BRCA2, CHEK.
Положительный опыт врачей клиники в лечении онкологических заболеваний — результат профессионализма и вдумчивого отношения к каждому конкретному пациенту. Врач-онколог, радиолог, химиотерапевт Маргарита Олеговна Скорина анализирует опыт лечения наиболее часто встречающегося у женщин заболевания — рака молочной железы.
— Чрезвычайно важно раннее выявление опухолевого процесса, так как это позволяет провести радикальное лечение, что даёт возможность значительно улучшить результаты и прогноз заболевания, позволяет использовать органосохраняющие операции. Например, для долькового и протокового рака in situ — TisN0M0 возможно выполнение лампэктомии, секторальной резекции молочной железы, резекция молочной железы подмышечной лимфаденэктомией, обязательно выполнение срочного гистологического исследования краёв резекции, возможна корректирующая операция на контралатеральной молочной железе. Обязательно проведение курса лучевой терапии на оставшуюся часть молочной железы РОД2Гр СОД 50 Гр, возможно гипофракционирование РОД 2,5 Гр СОД45 Гр, при наличии признаков сосудистой инвазии, опухолевых клеток в краях резекции, G 3, а также молодым пациенткам моложе 50 лет проводится облучение клиппированного ложа опухоли РОД 2 Гр СОД 10–16 Гр. При глубине залегания опухоли более 28 мм от кожи дополнительно применяется внутритканевая лучевая терапия РОД5–12Гр. Для стадий IIА T1N1M0 и IIВ T2–3N0M0 возможно выполнение резекции молочной железы с подмышечной лимфаденэктомией, подкожная или кожесохранная мастэктомия с одномоментной или отсроченной реконструкцией, мастэктомия с подмышечной лимфаденэктомией, также обязательно выполнение срочного гистологического исследования краёв резекции, возможна корректирующая операция на контралатеральной молочной железе. При кожесохранной мастэктомии и показаниях к проведению лучевой терапии — размер опухоли более 5 см, наличие опухолевых клеток на расстоянии менее 1 мм от края резекции — проводится лучевая терапия РОД 2 Гр СОД 48–50 Гр, при поражении 1–3 л/у, молодым пациенткам при G3 целесообразно включение в зону облучения передней грудной стенки и шейно-надключичной зоны. До хирургического лечения обязательна консультация радиолога, так как реконструктивный этап целесообразно провести по завершении курса лучевой терапии. Адъюватная лекарственная терапия подбирается исходя их биологического подтипа опухоли: Люминальный А — в большинстве случаев эндокринотерапия, Люминальный В Her2 отрицательный — химиотерапия для большинства больных с использованием антрациклинов и таксанов, эндокринотерапия всем больным; Люминальный В Her2 положительный — химиотерапия с использованием антрациклинов, таксанов, анти-Her2-терапия, эндокринотерапия. Her2 позитивный, нелюминальный — химиотерапия с использованием антрациклинов, таксанов и анти-Her2-терапия. Тройной негативный — химиотерапия с использованием антрациклинов и таксанов. К местнораспространённому раку молочной железы относят стадии IIIA, IIIВ, IIIС T0–2N2M0 T3N1–2M0 T4а, в, dN0–2M0, T любая N3 M0. Лечение проводят комбинированным методом: предоперационное лекарственное лечение, при наличии положительного ответа хирургического лечения, послеоперационная лучевая терапия, лекарственная терапия по показаниям. При отсутствии эффекта на первую линию лекарственного лечения возможно применение альтернативного лекарственного лечения, при отсутствии эффекта лучевая терапия проводится до хирургического этапа лечения, далее продолжается по индивидуальной программе. Основной целью лекарственной терапии и при первично неоперабельном раке молочной железы является уменьшение размеров опухоли с целью достижения операбельного состояния. Лечение проводится по тем же принципам, что и первично операбельного рака молочной железы. При успешно проведённом лекарственном лечении проводится мастэктомия с подмышечной, подлопаточной и подключичной лимфаденэктомией, объём оперативного вмешательства определяет хирург в зависимости от расположения опухоли, соотношения размера опухоли и объёма молочной железы. После проведения радикальной мастэктомии или органосохраняющих операций показан курс лучевой терапии на мягкой ткани грудной клетки зоны регионарного лимфооттока РОД 2 Гр СОД50 Гр. При наличии оставленных поражённых надключичных и подключичных л/у возможно их локальное облучение до СОД 60–645 Гр. Предоперационный курс лучевой терапии на молочную железу, все зоны регионарного лимфооттока на ипсилатеральные и парастернальные л/у РОД 2,5 Гр СОД 40–45 Гр (11). В случае неоперабельного опухолевого процесса или отказе от хирургического лечения возможно проведение радикального курса лучевой терапии РОД 2,5 Гр СОД 50–55–60 Гр, затем локально на опухоль до СОД 60–65–70 Гр, зоны лимфооттока РОД 2,5 Гр СОД 40–+50 Гр, локально на определяемые поражённые л/у до СОД 55–50–65 Гр.
Отдалённые результаты лечения принято оценивать по пятилетней выживаемости, которая напрямую зависит от стадии заболевания, при которой начато лечение. Современные методы лечения позволяют достичь пятилетней выживаемости при I стадии у 96 %, IIА стадии — 90 %, IIВ стадии — 80 %, IIIА стадии — у 87 %, IIIВ стадии — у 67 % больных.
К сожалению, на долю III и IV стадий рака молочной железы в нашей стране приходится более 30 % вновь выявленных случаев. Для диссеминированных форм рака молочной железы противоопухолевое лечение является паллиативным и направлено на улучшение качества жизни и увеличение её продолжительности. На сегодняшний день для Люминальных А и В опухолей назначается всем больным диссеминированным раком молочной железы, за исключением быстро прогрессирующих опухолей и болезни, осложнившейся висцеральным кризом, при которых необходимо быстрое достижение эффекта. При выборе варианта гормонотерапии следует учитывать функцию яичников (пре- и постменопауза), предшествующую гормонотерапию и её эффективность, сопутствующую патологию. Стандарта химиотерапии первой линии рецидивного и метастатического рака молочной железы нет. Выбор режима должен быть индивидуальным и учитывать особенности опухоли больного, а также эффективность предшествующего лекарственного лечения. Больные с Her2-положительным раком молочной железы должны получать анти-Her2-терапию в сочетании с химиотерапией или гормонотерапией.
Хирургические вмешательства проводятся у 30–40 % всех больных с раком молочной железы на поздних стадиях. При распадающихся опухолях с формированием язв, при массивных кровотечениях, с целью купирования кровотечения, предотвращения развития инфекционных осложнений и септического шока проводятся паллиативные санационные мастэктомии, при которых проводится полное или частичное удаление ткани молочной железы, а также окружающих тканей — фасций большой и малой грудных мышц, соединительной ткани; резекция регионарных лимфоузлов. Особую сложность представляет оказание помощи больным, не подлежащим хирургическому лечению из-за распространённости опухолевого процесса или при неэффективности проводимой терапии. В этом случае рассматривается вопрос о проведении фотодинамической терапии. Введённые в организм молекулы фотосенсибилизатора избирательно фиксируются на мембранах опухолевых клеток и митохондриях. Причём максимальная концентрация препарата в тканях достигается через 24–72 часа. При облучении фотосенсибилизированной опухолевой ткани лазерным излучением происходит переход нетоксичного триплетного кислорода (IIIO2) в синглетный (I O2) кислород, обладающий выраженным цитотоксичным действием, что приводит к разрушению клеточных мембран опухолевых клеток. Синглетный кислород, несмотря на короткое время действия, успевает полностью разрушить опухолевые клетки. При этом цитотоксический эффект зависит от концентрации фотосенсибилизатора, глубины проникновения света в ткани опухоли (14). Уже после первого сеанса достигается частичная остановка кровотечения из опухоли. Иногда у пациенток с большими по объёму опухолями для полного облучения всей поверхности требуется несколько сеансов. В этом случае сначала облучают наиболее кровоточащие участки. В процессе лечения происходит очищение опухоли от некротических масс, что приводит к исчезновению зловонного запаха распадающейся опухоли и формированию плотного струпа к 7–8 суткам после начала лечения. Купируется воспалительный отёк молочной железы. Из негативных факторов в процессе лечения отмечается усиление боли в области опухоли.
Проведение дистанционной лучевой терапии при распадающихся опухолях молочной железы невозможно ввиду высоких рисков кровотечения.
Современные информационные системы широко освещают достижения и успехи современной онкологии при раннем выявлении опухолевого процесса, для большинства пациентов понятна необходимость ранней диагностики и лечение опухолевого заболевания. Однако остаётся ряд пациентов, которые не спешат прибегать к медицинской помощи. Особого внимания врачей и клинических психологов требует этап диагностики и лечения, на котором больной узнаёт от врача и всё в большей и большей мере осознаёт, что болен тяжёлой болезнью, несущей угрозу его благополучию и самой жизни, требующей проведения труднопереносимого лечения (операция, химиотерапия, длительный постельный режим). Это вызывает у больного тревожные опасения за жизнь и здоровье, мрачные размышления о будущем, подавленность, страх перед возможной инвалидностью, ощущение краха карьеры, а подчас и всей жизни. Боль, слабость, физический дискомфорт усугубляют реакцию больного на психическую травму, в роли которой выступает тяжёлое и опасное заболевание. Выделяются как адекватные, так и патологические личностные реакции на болезнь и лечение, а также связанные с ними реальные и/или ожидаемые последствия. Личностная реакция квалифицируется как адекватная, если:
а) поведение больного, его переживания и представления о болезни соответствуют полученной от врача информации о тяжести заболевания и лечения, а также их возможных последствиях; б) больной соблюдает режим, следует предписаниям врача; в) больной в состоянии контролировать свои эмоции.
При выявлении представленной ниже психопатологической симптоматики у онкологических больных ставится диагноз невротической реакции на заболевание (реакции на тяжёлый стресс и нарушения адаптации, раздел F43 МКБ 10) или нозогении.
Наиболее часто в онкологии встречается депрессивная, фобическая и анозогнозическая реакция. Проявляется сниженным настроением, пессимистической оценкой перспективы, внутренней напряжённостью, предчувствием надвигающейся беды. Отмечается отрицание болезни с игнорированием лечебных рекомендаций и грубыми нарушениями режима, характерен страх перед лечением, опасения прогрессирования процесса, метастазированием опухоли, внезапной смертью. Приведённые психологические реакции характерны для преморбидно психически здоровых лиц. Спустя несколько месяцев личностные реакции на болезнь и её последствия постепенно исчезают. Через 6–12 месяцев от начала заболевания или физической травмы у большинства больных наступает психологическая реадаптация, приспособление к изменившимся условиям жизни. У остальных больных психические изменения, связанные с тяжёлой травмой, с труднопереносимым лечением, возникновением и развитием онкологического, соматического или неврологического заболевания, подчас вразрез с удовлетворительным соматическим состоянием, усугубляются, закрепляются, формируются неврозы. В некоторых случаях в отдалённом периоде после начала заболевания или физической травмы наблюдается патологическое развитие личности больного с «уходом в болезнь»: сужение круга интересов (ограниченных состоянием своего здоровья и проблемами, связанными с лечением), нарушение социальных связей и социальной самоизоляцией, рентными установками.
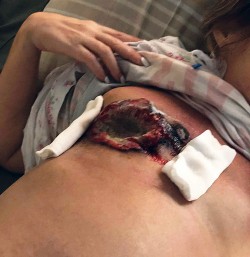
Клинический пример проявления анозогностического типа реакции пациентки с диагнозом рак правой молочной железы с распадом с T4сN3M1 (тотальное Mts поражение печени, Mts в аксиллярные, надключичные л/у справа, парастернальный л/у справа, множественное поражение костей скелета, лёгкие) 4-й стадии.
Больная Н. 59 лет. Из анамнеза: больной себя считает около 7 лет, когда в 2012 году самостоятельно обнаружила опухолевидное образование в правой молочной железе. К врачам не обращалась, «подозревала, что образование в правой молочной железе — опухоль, но не придала этому значения, не было времени идти в поликлинику» (со слов больной). На протяжении этого времени опухоль увеличивалась в размерах, несколько лет назад (точно не помнит) на месте опухоли образовалась кровоточащая зловонная язва, которая увеличивалась в размерах, приблизительно в то же время образовалось плотное несмещаемое опухолевидное образование по передней подмышечной линии, которое также увеличивалось в размерах. В течение этого времени больная регулярно посещала терапевта, косметолога, однако от проведения рутинных скрининговых обследований отказывалась. Соматически отягощена артериальной гипертензией 1-й степени, по поводу которой регулярно принимала гипотензивные препараты. В марте 2019 года отметила появление тошноты, рвоту съеденной пищей, снижение аппетита, появилась слабость, живот увеличивался в размерах. Обратилась в частную многопрофильную клинику г. Москвы: осмотрена онкологом, предположительный диагноз — распадающийся рак правой молочной железы; от проведения гистологического исследования и противоопухолевого лечения отказалась, в виду страха перед проведением химиотерапии и потерей волос; по мнению пациентки, врач не проявил должного сочувствия, запугивал осложнениями химиотерапии. В последние месяцы отметила ухудшение самочувствия, тошнота стала постоянной, участилась рвота, в течение последнего месяца отметила резкое увеличение живота в объёме, опухолевая язва в области правой молочной железы стала обильно кровоточить, самостоятельно применяла гемостатическую губку, перекись водорода — без эффекта. По совету знакомых применяла нетрадиционную медицину: использовала заживляющую мазь для собак (название не помнит), также без эффекта. При осмотре: молочная железа слева соответствует полу и возрасту, сосок и ареола нормальной окраски. Ареола соска не приподнимается над поверхностью железы. При пальпации ткань левой молочной железы однородной железистой консистенции, дополнительные образования чётко не пальпируются. Отделяемого из соска левой молочной железы нет. На месте правой молочной железы кратерообразная безболезненная язва до 12 х 10 см, с подрытыми обильно кровоточащими краями и налётом серого фибрина в дне язвы, с гнилостным запахом, глубиной до 2,0 см, в дне раны пальпируется ребро. В проекции 2–3-го межрёберья справа по переднее подмышечной линии крупный вколоченный конгломерат л/у до 4,5 х 3,0 см. Кожа над ним без изъязвлений, в аксиллярной области справа множественные увеличенные л/у до 2,0 см в диаметре. Остальные группы л/у чётко не пальпируются.
При дообследовании КТ ОГК и ОБП с контрастом определяется опухоль в области правой молочной железы 98 х 85 х 39 мм (поперечный, вертикальный, переднезадний размер). Структура солидная, несколько неравномерно накапливает контрастный препарат, в центральных отделах определяется язвенный дефект. Распространяется на кожу железы, на нижние отделы большой и малой грудной желёз справа, прилежит к передней поверхности межрёберных мышц в области передних отделов 4–5-го межрёберья справа, нельзя исключить инвазию. В медиальных отделах правой молочной железы определяется два опухолевых узла аналогичной структуры, размерами 16 х 16 мм (распространяется на большую грудную мышцу) и 20 х 28 мм (распространяется на кожу). Большинство поражённых подмышечных л/у сливаются в конгломерат размерами до 33 х 51 х 52 мм. Одиночный правый надключичный л/у до 7 х 10 мм, левые надключичные л/у до 5 мм, одиночный правый парастернальный л/у на уровне опухоли до 5 х 10 мм. В обоих лёгких определяются немногочисленные мелкие размером 2–3 мм очаги уплотнения. Определяется 2-сторонний небольшой гидроторакс, толщина слоя жидкости справа до 17 мм, слева до 10 мм. Визуализируются остеосклеротические очаги (наиболее вероятно, Mts природы в 3-м ребре справа, в 7-м ребре с обеих сторон, в телах Th 5, Th 6, Th 10Th 11 позвонков, размерами до 16 х 21 мм (Th 11). В отделах брюшной полости — свободная жидкость. Печень увеличена: вертикальный размер правой доли — 221 мм. В структуре многочисленные сливные Mts до 70 мм. В костях множественные бластические, литические и смешанные Mts до 33 мм. Патологический перелом верхней ветви правой лобковой кости.
Выполнена биопсия опухоли правой молочной железы. Гистология: инвазивный рак молочной железы, НСТ, с инвазией в жировую клетчатку, мышечную ткань, стенку сосудов, наличием опухолевых эмболов в просвете сосудов, распространёнными деструктивными изменениями. ИГХ — РЭ 8 б, РП 6 б, Her2 — 0, ki 67 — 10 %, РЭА 8888,0 нг/мл, СА 15–3 9930 ед/мл.
В биохимическом анализе крови гипопротеинемия 1-й стадии, гипербилирубинемия выше 3 ВГН, повышение АДТ и АСТ, ЩФ выше 6 ВГН. В общем анализе крови анемия 1-й степени.
По данным МРТ головного мозга с контрастом, патологических изменений головного мозга не выявлено.
Консультация психиатра — эндогенная депрессия, анозогнозия.
Пациентка ознакомлена с результатами инструментальных и лабораторных обследований, однако не проявила интереса к возможным вариантам лечения и прогнозу, в стационаре проводилась симптоматическая, гемостатическая, гепатопротекторная, дезинтоксикационная терапия, без особого эффекта, на 7-й день от момента верификации диагноза больная скончалась.
Опыт лечения пациентки с явной анозогностической реакцией на опухолевое заболевание доказывает необходимость участия в лечении психолога. Психокоррекционную работу следует проводить и с членами семьи больного, в первую очередь с супругами и детьми больных. Это необходимо для формирования у лиц ближайшего окружения больного адекватных представлений о болезни, путях её преодоления и последствиях.
Амбулаторному терапевтическому и хирургическому звену следует обращать особое внимание на пациенток, отказывающихся от прохождения скрининговых обследований, консультаций маммолога, стараться уточнять истинную причину отказов, стараться привлекать психологов к работе с такими пациентами. Учреждениям, занимающимся лечением онкопациентов, необходимо иметь штатного психолога/психиатра для своевременной и эффективной психологической помощи больным и их близким.






.jpg)
 8(495)258-97-03
8(495)258-97-03 